左全肺切除的手术入径和方法
手术方法
术前准备
所有患者术前均需进行软性或者硬性支气管镜检查。术中双腔插管,左肺隔离,保证左主气管没有异物。
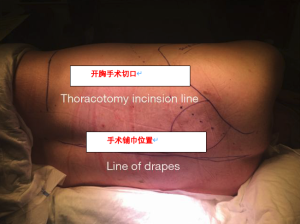
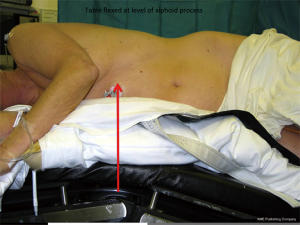
确认左肺隔离完全后,右侧卧位。右膝关节弯曲90°,左下肢伸直,两腿之间垫软枕。双侧上臂呈“祈祷”样弯曲,充分暴露左侧腋窝,无需将左上臂固定于固定架。剑突水平位置弯曲手术床,尽可能扩大肋间隙(图1)。患者使用环绕骨盆的安全带和特殊的袋子进行固定,确保不会滚落床下。术前患者自左肩部到骨盆上,脊柱到前侧胸骨包括左侧腋下都需要消毒,之后在这些部位铺巾单。
切口
可以通过前外侧或者后外侧切口进胸。
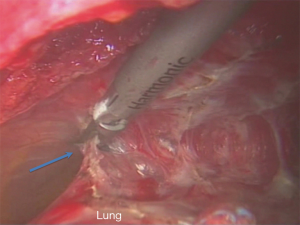
我们中心推荐后外侧切口进胸,因为便于保证肋骨结构完整,并且对听诊三角的肌肉损伤最小(图2)。
粘连并不是手术禁忌证,但是需要额外注意:(Ⅰ)清晰分辨术中所见平面;(Ⅱ)粘连分离时注意及时止血,保证术野干净;(Ⅲ)避免脏层胸膜破裂;(Ⅳ)充分的分离粘连,保证游离整个肺部,彻底游离肺门结构。
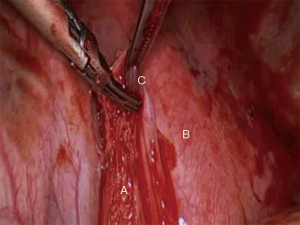
如果以上操作不能实现,则需要额外的胸膜外剥离。主刀医生要确保能够完整切除肿瘤,切缘足够,保证阴性(图3)。
手术
肺癌导致的全肺切除手术,需要全面的胸膜腔检查,排除可能的胸膜转移灶。同时,任何癌症术中发现的可疑胸腔积液都需要送细胞学检测[1,2]。
肺门分离[3]
这步手术操作有以下几个要点:(Ⅰ)评估肺门的结构;(Ⅱ)辨认和保护纵隔内的结构;(Ⅲ)评估肿瘤切除的可能性;(Ⅳ)是否需要进行淋巴结切除或者淋巴结采样。
一助牵拉左肺,暴露术野后在左肺动脉水平进行肺门解剖。在主-肺动脉窗位置打开胸膜,切除脂肪和结缔组织,同时使用夹子或者结扎处理迷走神经分支及其伴行的小血管。此区域靠近左侧喉返神经,因此不建议使用电凝类止血器械[3,4]。
钝性分离左肺动脉主干后进行游离,使用手指轻柔的环形分离或者手术钳夹纱布制成的“花生米”进行钝性分离左肺动脉,格外注意不要损伤静脉。完整游离肺动脉后使用血管套带牵拉,确认无误后用血管钳伸入后方,带入血管套带后,将套带留置。在肺门和食管之间的间隙继续向后、向下分离,可见支气管血管和左侧迷走神经较大的分支,我们倾向单独结扎分支和血管后,牵拉断端,方便从肺门悬吊暴露后纵隔。此时在肺动脉和气管间隙当中切除第十组淋巴结,注意止血。
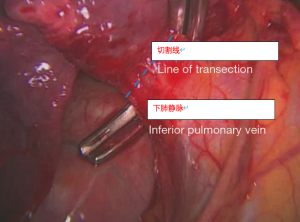
进一步向下分离,暴露左下肺静脉。左下肺静脉完整暴露后,即可分离松解左下肺韧带并完成第九组淋巴结的切除(图4)。此时能够轻松的用手指钝性分离下肺静脉周围,然后血管钳(图5)伸入后方带入血管套带,保留套带在胸腔。
侧方牵拉肺部,暴露肺门前方,辨认膈神经,在肥胖患者当中,它有时行走在心包脂肪组织当中。采用钝性分离方式将其从肺门当中分离,这里的解剖游离不要使用电凝、高温类器械,以防损伤神经[5,6]。
完整的游离暴露肺门最后的血管上肺静脉,上肺静脉会有分支并且较粗,我们可以用食指和拇指小心的牵拉游离好的肺动脉,暴露间隙,从而便于从上肺静脉的最上端进行游离,然后使用血管套带。
此时剩下左主支气管,但是因为肺门血管的包绕,解剖位置深,很难解剖游离。各种各样的技术手段和器械能够游离肺血管。目前,最简单和最高效的技术手段是使用腔内血管切割吻合器,它们可以很方便的在开胸切口的手术视野中使用,并且能够顺着之前的血管套带或者吊带,在后方滑入血管进行离断。
如果外科医生希望使用小切口完成开胸手术,可以使用前侧的小切口置入切割吻合器,手术后该切口可以作为胸管置入的切口[7]。
我们建议先切断肺动脉,以防肺静脉切断后肺部淤血[8]。使用血管套带牵拉肺动脉,打开切割吻合器钳口缓慢滑入血管,将血管置于上下钉钻之间。喜欢小切口开胸的医生,此时操作的视野会比较困难。在这种小开胸的情况下,右手食指可以放在肺动脉周围,作为吻合器钳口的引导,以便安全的穿过肺动脉。使用吻合器前要充分的预估肺动脉的粗细,选用合适的钉仓。要尽可能的在近心端闭合血管,避免出血。
使用切割吻合器由心包方向往后纵隔闭合下肺静脉。切割闭合器击发之前,确保血管套带离开血管,避免血管套带被卡在闭合后的静脉残端。
上肺静脉采用类似的操作方法处理。此时仅仅依靠支气管连于肺门的肺能够被轻松的切掉。
如果患者负担不起直线切割吻合器的费用或者不能使用直线切割吻合器,经典的缝合和结扎也是可以替代的。一般来说,肺动脉可以使用2把血管钳钳闭,整齐的切断,然后使用不可吸收的单丝线和无损伤针头缝合(如4/0普理灵缝线)。静脉可以采用类似方法处理。我们不建议采用单纯结扎处理血管,因为术后线结容易松散导致大出血。我们的经验表明因为心包近段残端回缩,肺静脉更容易出现这类大出血,导致结扎存在风险。
血管远端残端可以结扎,但是我们仍然推荐缝扎,因为远端的出血仍然会导致术者的不适,扰乱手术操作流程,最后导致出现血淋淋且糟糕的术野。
综上所述,支气管可以用直线切割吻合器或者缝扎方式处理。
切割闭合气管前,针对肺癌患者要仔细处理隆突下淋巴结。气管周围的脂肪和结缔组织要清扫干净,确保切割到隆突区域。这样的操作可以保证直线切割吻合器到达最佳切割位置,以防气管残端过长。向后牵拉余肺,从下往上置入直线切割吻合器。有时直线切割吻合器可以抵至主动脉弓,保证最短的支气管残端。
切割闭合器通常会将气管前壁和膜部相互压缩,在切割闭合时,牵拉好余肺,减小肺的张力,以免切割气管后导致气管破裂。
如果采用缝合处理支气管,不要直接切断支气管,避免气管内的细菌进入胸腔播散。使用特别设计的弧形支气管夹,尽可能的在隆突下处理。支气管切断后,将肺从胸腔中取出。
保持支气管夹在原位,三角针带单丝或者多丝丝线进行双重水平褥式缝合[9]。有足够的文献证据支持,采用单丝或者多丝丝线缝合成功的前提包括:(Ⅰ)良好的支气管壁完整性[10];(Ⅱ)支气管壁组织的血供正常和健康,不要缝合的过密;(Ⅲ)支气管残端短。由于支气管残端一般是被纵隔的组织结构覆盖,一般是不需要专门去包绕覆盖左主支气管残端,除非出现以下情况[11,12]:(Ⅰ)支气管组织活性不好;(Ⅱ)患者术前接受过化疗和/或放疗;(Ⅲ)患者需要进行新辅助化疗和/或放疗;(Ⅳ)患者的胸腔伴有感染或者炎症;(Ⅴ)患者营养状况较差。
术后
接下来或者完成淋巴结切除术后,使用无菌生理盐水冲洗胸腔[13,14]。检查支气管残端是否漏气。如果漏气,需要缝合支气管残端。
全肺切除术后是否需要留置胸管仍然存在显著争论。但是只要遵循合适的治疗原则,任何一种治疗方式都是安全有效的。
在我们中心,术后常规留置一根胸管到手术后第一天(POD1)。我们的治疗原则包括:(Ⅰ)患者手术结束后转为仰卧位后夹闭胸管;(Ⅱ)每小时开放一次胸管,观察胸管引流;(Ⅲ)确认无引流后及时夹闭胸管;(Ⅳ)手术次日(POD1)拔除胸管。
Acknowledgments
Funding: None.
Footnote
Provenance and Peer Review: This article was commissioned by the Guest Editors (Marco Scarci, Alan D.L. Sihoe and Benedetta Bedetti) for the series “Open Thoracic Surgery” published in Shanghai Chest. The article has undergone external peer review.
Conflicts of Interest: Both authors have completed the ICMJE uniform disclosure form (available at http://dx.doi.org/10.21037/shc.2017.08.10). The series “Open Thoracic Surgery” was commissioned by the editorial office without any funding or sponsorship. The authors have no other conflicts of interest to declare.
Ethical Statement: The authors are accountable for all aspects of the work in ensuring that questions related to the accuracy or integrity of any part of the work are appropriately investigated and resolved.
Open Access Statement: This is an Open Access article distributed in accordance with the Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), which permits the non-commercial replication and distribution of the article with the strict proviso that no changes or edits are made and the original work is properly cited (including links to both the formal publication through the relevant DOI and the license). See: https://creativecommons.org/licenses/by-nc-nd/4.0/.
References
- Saso S, Rao C, Ashrafian H, et al. Positive pre-resection pleural lavage cytology is associated with increased risk of lung cancer recurrence in patients undergoing surgical resection: a meta-analysis of 4450 patients. Thorax 2012;67:526-32. [Crossref] [PubMed]
- Shoji F, Yamazaki K, Kouso H, et al. The Impact of Pleural Lavage Cytology Both Before and After Lung Resection on Recurrence of Non-Small Cell Lung Cancer. Ann Thorac Surg 2016;101:2141-6. [Crossref] [PubMed]
- Nohl-Oser HC, Nissen R, Schreiber HW. Surgery of the lung. Stuttgart, New York: Thieme-Stratton, 1981:79-90.
- Filaire M, Mom T, Laurent S, et al. Vocal cord dysfunction after left lung resection for cancer. Eur J Cardiothorac Surg 2001;20:705-11. [Crossref] [PubMed]
- Burns J, Dunning J. Is the preservation of the phrenic nerve important after pneumonectomy? Interact Cardiovasc Thorac Surg 2011;12:47-50. [Crossref] [PubMed]
- Kocher GJ, Mauss K, Carboni GL, et al. Effect of phrenic nerve palsy on early postoperative lung function after pneumonectomy: a prospective study. Ann Thorac Surg 2013;96:2015-20. [Crossref] [PubMed]
- Ugalde P, Miro S, Provencher S, et al. Ipsilateral diaphragmatic motion and lung function in long-term pneumonectomy patients. Ann Thorac Surg 2008;86:1745-51; discussion 1751-2.
- Szwerc MF, Landreneau RJ, Santos RS, et al. Minithoracotomy combined with mechanically stapled bronchial and vascular ligation for anatomical lung resection. Ann Thorac Surg 2004;77:1904-9; discussion 1909-10.
- Refaely Y, Sadetzki S, Chetrit A, et al. The sequence of vessel interruption during lobectomy for non-small cell lung cancer: is it indeed important? J Thorac Cardiovasc Surg 2003;125:1313-20. [Crossref] [PubMed]
- Scott RN, Faraci RP, Hough A, et al. Brochial stump closure techniques following pneumonectomy: A serial comparative study. Ann Surg 1976;184:205-11. [Crossref] [PubMed]
- Kakadellis J, Karfis EA. The posterior membranous flap technique for bronchial closure after pneumonectomy. Interact Cardiovasc Thorac Surg 2008;7:638-41. [Crossref] [PubMed]
- Panagopoulos ND, Apostolakis E, Koletsis E, et al. Low incidence of bronchopleural fistula after pneumonectomy for lung cancer. Interact Cardiovasc Thorac Surg 2009;9:571-5. [Crossref] [PubMed]
- Lardinois D, Horsch A, Krueger T, et al. Mediastinal reinforcement after induction therapy and pneumonectomy: comparison of intercostal muscle versus diaphragm flaps. Eur J Cardiothorac Surg 2002;21:74-8. [Crossref] [PubMed]
- Tsakok T, Tsakok M, Damji C, et al. Washout after lobectomy: is water more effective than normal saline in preventing local recurrence? Interact Cardiovasc Thorac Surg 2012;14:200-4. [Crossref] [PubMed]

夏迎晨
2019年始就读于南昌大学医学部胸外科专业,博士生导师喻本桐教授。
2020.12-2021.12公派西班牙巴塞罗那PRBB研究所从事肺癌、支扩等研究。
主持江西省研究生创新基金一项(YC-2020-B056),参与多项国自然项目。以第一作者身份在Cell Death & Disease、Frontiers in oncology 等杂志发表多篇文章。(更新时间:2021/7/28)
(本译文仅供学术交流,实际内容请以英文原文为准。)
Cite this article as: Kostoulas N, Papagiannopoulos K. Open surgical approach and technique in left pneumonectomy. Shanghai Chest 2017;1:23.